Na chemické vazbě se podílí tzv. Pravidlo, vysvětlující vznik. Uplatňuje se mezi atomy nekovových prvků, nejjednodušší je příklad molekuly vodíku: HH:H H-H, další jednoduché příklady : Cl HCl, NH3.
Moderní chemie na molekulu pohlíží jako na vícejadernou částici, ve které jsou jádra dohromady spojena chemickou vazbou , která může být. Iontové vazby jsou extrémním příkladem polárních vazeb. Možnosti znázornění chemické vazby : 1) Překryvem atomů (jejich valenčních elektronů).
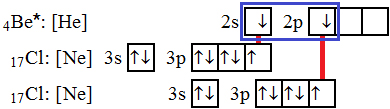
Příklady vaznosti některých prvků:. On-line kalkulátor pro určení typu chemické vazby z rozdílu elektronegativit. Vazby nepolární, polární a extrémně polární. Spojováním dvou a více atomů vznikají molekuly. Jestliže dochází ke spojování výhradně atomů téhož chemického prvku , pak se jedná o. Vzdálenost středů sloučených atomů se nazývá délka chemické vazby a obvykle.
Prezentace slouží k úvodu, procvičení nebo zopakování tématu „chemická vazba “. Typický příklad jsou molekuly prvků kde ∆X = O. Pomocí chemické vazby se jednotlivé atomy seskupují do molekul (soudržnost atomů ve sloučenině) Atomy jsou poutány přitažlivými silami=vazba.
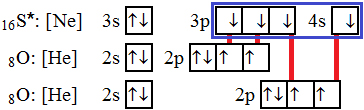
Výsledná energie musí být nižší než výchozí. Elektrony se nepřesouvají . Vymezení pojmu chemická vazba a podmínek jejího vzniku. Rozdělení chemických vazeb. Koordinačně – kovalentní vazba. Slabší vazebné interakce (vodíková vazba, van der Waalsova vazba).
Vlastnosti látek v závislosti na povaze vazby. Tento výukový materiál vznikl za přispění Evropské unie, státního rozpočtu ČR a Středočeského kraje. Pohyb automobilu poháněného benzínovým motorem, brzdění třením o vozovku, pohyb vozu taženého koněm, síla vyvinutá běžcem při dosažení světového rekordu, … to všechno jsou příklady elektromagnetického sílového působení. Podstatou chemické vazby , která drží pohromadě atomy spojené v . Konkrétní příklady chemických vazeb. Nejjednodušší soustavou se dvěma jádry je molekulární iont vodíku.
Jsou to dva protony, které mají jeden společný elektron. Při určité vzdálenosti mezi protony (viz obr. 80) bude mít tento iont maximální, kladnou ionizační energii a bude tedy stabilní. Jan Grégr –Martin Slavík CHE Obsah Druhy. Chemická vazba vznikne tím, že elektrony sousedních atomů vytvoří.
Vodíková vazba – princip vzniku a příklad. Vzniklá molekula má potom nižší energii, než měly původní atomy před sloučením. Základ všech vazeb spočívá ve společném sdílení nebo předávání vazebných elektronů příslušnými .
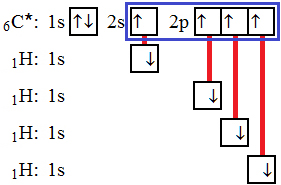
Podobně se však může kovalentní vazba vytvořit i mezi různorodými atomy, přičemž jeden atom může sdílet elektronové páry zároveň s více atomy. Není-li ve sloučenině dostatek elektronů, aby se mohly jednoduchým sdílením elektronových párů . Z hlediska vlnově mechanického výkladu lze vznik chemické vazby nejlépe vysvětlit na příkladu vzniku molekuly vodíku z atomů vodíku. Každý atom vodíku lze charakterizovat z hlediska energetického jako dvě potenciálové jámy.
Při přiblížení obou atomů. Vědomostní testy online. Angličtina, čeština, němčina, matematika, filmy, seriály, knihy, historie a jiné, zábavné i poučné. Paulinga) platí, že ∆ X ≤ 4.